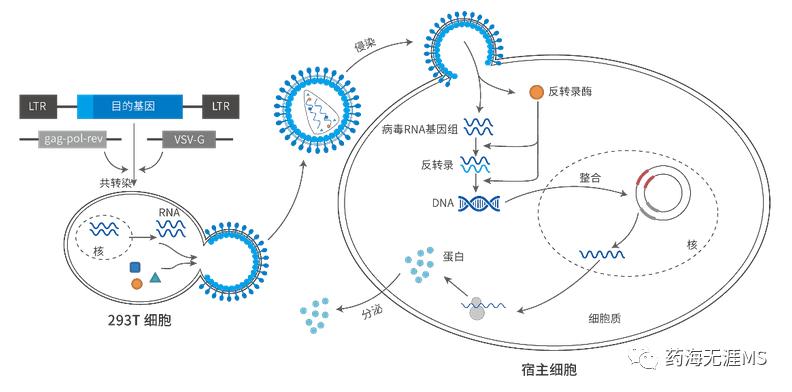
基因治疗的实施是一项相当复杂的挑战,载体的选择尤为重要,载体主要有两个重要功能——一个是保护壳内的脆弱货物,第二个是其表面配体与特定细胞相互作用。基因治疗载体分为病毒载体和非病毒载体,本篇我们将详细介绍病毒载体。
腺病毒
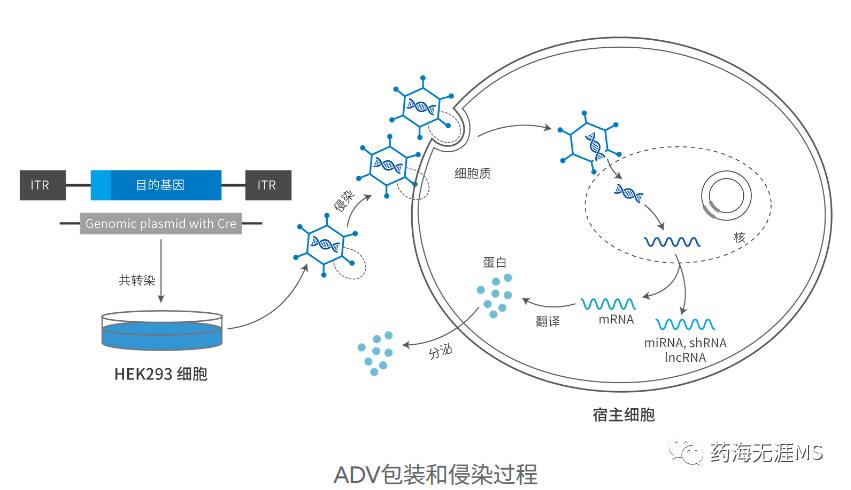
腺病毒(Adenovirus, ADV)是一种无包膜的线性双链DNA病毒,具有广泛的细胞和组织感染能力。感染过程剧烈,适于短时间内进行基因高表达的实验,与其它病毒相比,腺病毒优势在于插入片段较长,表达活性强。
体外应用时,腺病毒载体转基因效率高(接近100%的转导效率),且可转导不同类型的细胞,对于大量难转染细胞的基因递送是一个很好的工具。但是,在体内应用时,由于腺病毒免疫原性强,感染剧烈,故常会引起动物局部组织炎症反应和机体免疫反应,对动物体征和实验结果的客观性造成影响。
腺病毒包装骨架达质粒与穿梭质粒共转染HEK-293细胞,待细胞出现CPE状态后通过收集细胞上清和细胞裂解物,通过浓缩或氯化铯密度梯度离心纯化病毒。
CPE(Cytopathic Effect):病毒对组织培养细胞侵染后产生的细胞变性,利用此种病变效应可进行病毒定量。
腺相关病毒
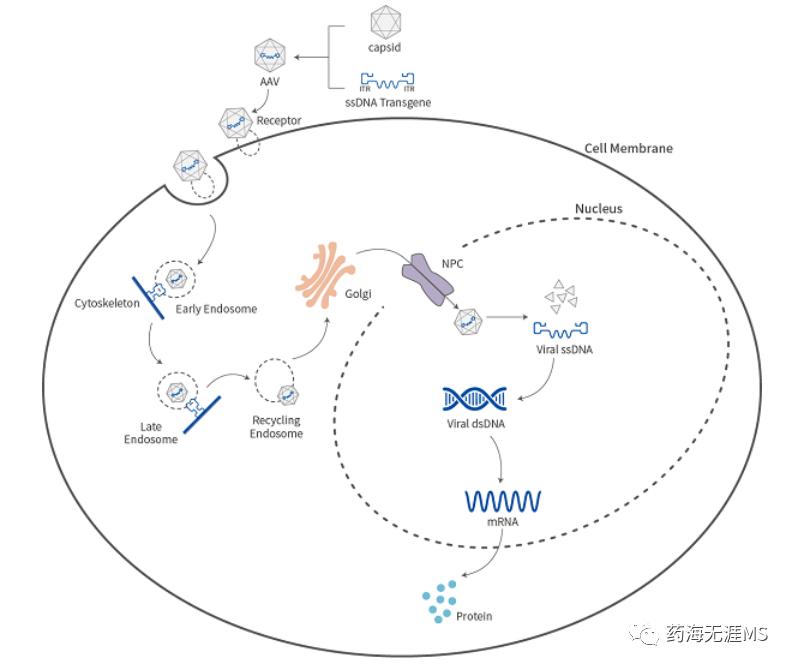
腺相关病毒(Adeno-associated virus,AAV)是微小病毒科(Parvoviridae)家族的成员之一,是一类无法自主复制、无被膜的二十面体微小病毒,其直径约20-26nm,含有4.7kb左右的线状单链DNA作为基因组。
重组腺相关病毒载体(recombination AAV, rAAV)是在非致病的野生型AAV基础上改造而成的基因载体,研究中采用的rAAV通常为AAV2型基因组与不同的衣壳蛋白结合产生的混合体病毒载体。
自互补AAV(Self-complementaryAAV,scAAV)是在rAAV的基础上将其编码区域设计成双链DNA,感染细胞后互补部分互补形成双链DNA,不需等待第二链DNA合成,取消了rAAV基因表达的限速步骤,因此scAAV感染后3-5天即可到达表达峰值。

rAAV载体优势
1、安全性高、免疫原性低:AAV是一种复制缺陷型DNA病毒,无自主复制能力,野生型AAV依赖rep基因进行低频定点整合,rAAV不整合。目前尚无由AAV引起的人类及哺乳动物疾病报道,也是FDA批准上市的基因治疗药物中最安全的病毒载体之一。
2、宿主细胞范围广:AAV具有广泛的宿主范围,对分裂细胞和非分裂细胞均具有感染能力。
3、扩散能力强:AAV直径约20-26nm,体积小,滴度高,具有良好的扩散能力,其中AAV-PHP.eB和AAV9具有跨血脑屏障的能力,在神经科学领域应用广泛。
4、体内表达基因时间长:AAV具有保持长期基因转录表达能力,体内表达一般3周可以达到高峰,随后持续高表达,作用时间>5个月。
5、种类多样:AAV血清型众多
慢病毒载体
慢病毒载体(Lentivirus)是一类改造自人免疫缺陷病毒(HIV)的病毒载体,是逆转录病毒的一种,基因组是RNA,其毒性基因已经被剔除并被外源性目的基因所取代,属于假型病毒可将外源基因整合到基因组中实现稳定表达,具有感染分裂期与非分裂期细胞的特性。
慢病毒基因组进入细胞后,在细胞浆中反转录为DNA,形成DNA整合前复合体,进入细胞核后,DNA整合到细胞基因组中。整合后的DNA转录成mRNA,回到细胞浆中,表达目的蛋白或产生小RNA。慢病毒介导的基因表达或小RNA干扰作用持续且稳定,并随细胞基因组的分裂而分裂。