癌症免疫疗法—mRNA
mRNA疗法因其可以在体内表达已知蛋白质的优越性,已经成为癌症免疫疗法的前沿研究领域。特别是通过小剂量的mRNA递送,抗原呈递细胞(APC)可以合成突变新抗原和多抗原,并将表位呈递给T淋巴细胞引发抗肿瘤作用。此外,在特定免疫细胞中表达CAR、TCR、CD134等受体以及细胞因子、干扰素和抗体等免疫调节因子,可以增强针对肿瘤的免疫反应。然而,由于将mRNA递送至靶器官或细胞以及mRNA的内体逃逸效率不足,基于mRNA抗癌策略的临床转化受到限制。
近年来,基于mRNA的癌症免疫疗法取得了一些进展,大致可分为mRNA结构的修饰和递送系统(尤其是脂质纳米颗粒平台)的开发。

最近,中科院上海药物研究所于海军研究员和华东师范大学徐志爱教授在Exploration发表了一篇题为“From structural design to delivery: mRNA therapeutics for cancer immunotherapy”的综述文章,重点介绍了克服基于mRNA的癌症免疫治疗瓶颈的策略,例如mRNA不稳定性、先天免疫原性和较低表达效率。此外,还强调了设计最佳递送平台将mRNA转运至特定位点的进展,按靶器官和细胞分类(图1),讨论了递送系统中特定分子结构的功能,特别是具有靶向递送特性的 mRNA 载体,还阐述了目前基于 mRNA 的癌症免疫疗法临床应用的挑战和机遇。
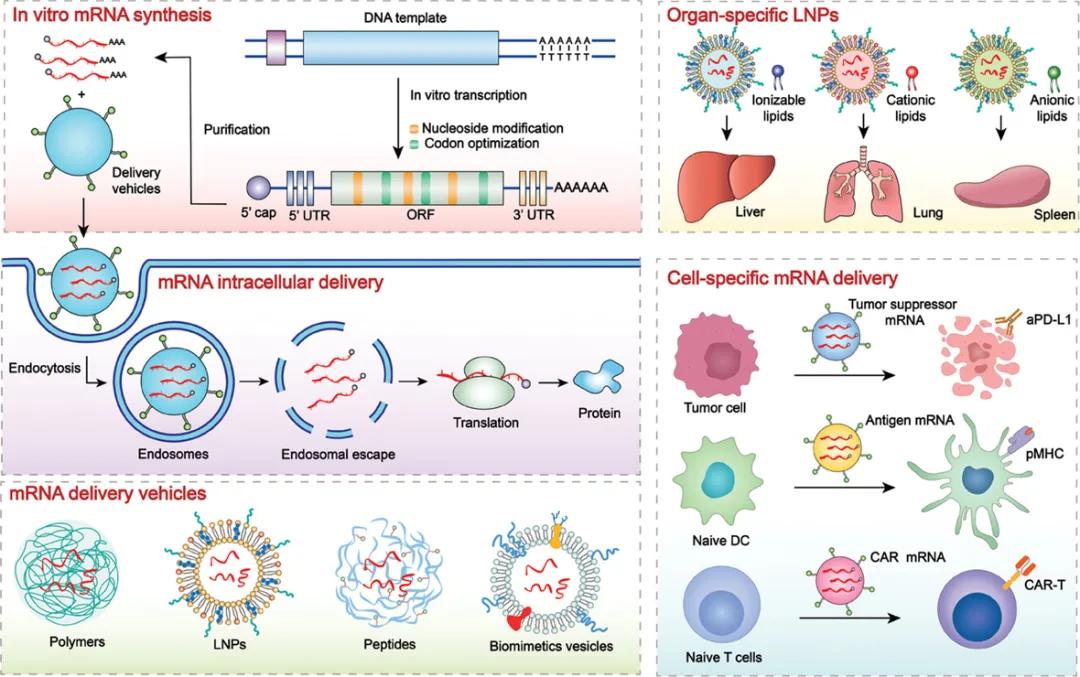
▲图1 mRNA化学修饰和组织/细胞靶向递送原理示意图
基于mRNA的癌症免疫治疗的分子设计
mRNA是一种带负电荷的单链RNA,含有从DNA转录而来的遗传信息,并依靠核糖体翻译成蛋白质以实现特定的生命功能。这种脆弱的大分子结构决定了mRNA在富含各种肽和酶的体内环境中不稳定。此外,聚阴离子mRNA会排斥带负电荷的细胞膜(CM),使其难以进入细胞。IVT方法利用噬菌体T7 RNA聚合酶(T7 RNAP)在线性化DNA模板的指导下高保真地合成mRNA,但由于天然来源的mRNA与合成的mRNA之间存在差距,mRNA的蛋白表达不够有效,需要对mRNA结构和核苷酸进行进一步修饰。此外,内体逃逸的低效率显著损害了RNA药物的功效。例如,FDA 批准的 DLin-MC3-DMA LNP 只能介导 1-4% RNA 释放到细胞质中。
mRNA的先天免疫原性是另一个需要考虑的问题。外源mRNA作为免疫原而不是治疗药物,这是由mRNA的先天免疫原性决定的。APC特别通过模式识别受体(PRR)如Toll样受体(TLR)识别IVT mRNA,刺激I型干扰素(IFN-I,包括IFN-α和IFN-β)和促炎因子的分泌,从而显著损害mRNA的蛋白质表达过程。此外,IFN-I对于癌症免疫疗法的表现既有利又有害。它促进树突状细胞 (DC) 成熟、抗原呈递给 T 细胞以及 CD8 + T 细胞的激活。另一方面,IFN-I可以增加Treg和Th17细胞的数量,诱导髓源性抑制细胞(MDSC)的瘤内浸润,促进肿瘤细胞的免疫逃逸。
在体内mRNA治疗的初期,注射到体内的mRNA会引起一系列异源免疫反应并被免疫系统裂解,就像机体正在对抗病毒的入侵一样,这极大地限制了mRNA治疗的应用。因此,克服mRNA免疫原性的技术突破至关重要。2005年,Katalin等人研究发现,用假尿苷替代尿苷可以降低mRNA激活DC的风险,不仅可以保护合成的mRNA免受免疫消除,还可以显著提高蛋白质表达的效率。这一发现解决了基于mRNA的治疗的担忧,从而拉开了mRNA临床应用的序幕。并在今年斩获诺贝尔生理学奖。除了核苷替换外,IVT-mRNA结构修饰还包括5'Cap、poly(A)尾和UTR。

▲图2 用于改进基于mRNA的癌症免疫治疗的mRNA结构修饰、佐剂添加、核苷修饰和密码子优化的示意图
提高mRNA稳定性和蛋白质表达效率的另一个策略是优化UTR序列,mRNA的UTR可分为5'和3'端。5' UTR 靠近 mRNA 的起始密码子,可以影响ORF翻译的速率。一份报告表明,没有复杂二级结构和起始密码子(如AUG和CUG)的较短5'UTR有利于启动mRNA的翻译过程,这些点在设计mRNA疫苗时值得考虑。3'UTR是常见的调控元件,也会影响mRNA的表达效率。有研究者筛选并获得了多个新型3'UTR,与一般3'UTR相比,显著提高了mRNA的蛋白翻译水平。
另外还有人通过分析内源基因表达并创新的设计UTR序列,筛选出了5' 和3' UTR的最佳组合,其蛋白质表达效率比内源UTR高5至10倍。此外,机器学习可以用于促进UTR序列设计。Castillo-Hair等人开发了一种基于实验数据训练的卷积神经网络模型,名为Optimus 5-Prime,该模型可以与算法相结合,从头设计UTR序列,提高翻译效率,加速在mRNA治疗中开发新型UTR的进程。
除此之外,mRNA的核苷修饰和密码子优化对于效率提升也很重要,例如5-甲基胞苷 (m5C)、N6-甲基腺苷 (m6A)、假尿苷 (Ψ)、5-甲氧基尿苷 (5moU) 和 1-甲基假尿苷 (m1 Ψ) 是用于mRNA重塑的主要修饰核苷酸,不仅提高了蛋白质翻译效率,还减少了mRNA的先天免疫激活。而由于密码子的简并性,同一蛋白质氨基酸序列存在数以亿计的密码子组合和二级结构,导致筛选具有最佳稳定性和翻译效率的mRNA核苷酸序列费时费力。最近,百度推出一种名为 LinearDesign 的人工智能 (AI) 和动态编程算法,可以缩短这个筛选过程,允许在大约十分钟内发现具有最佳序列的mRNA。
mRNA的癌症免疫治疗的递送系统
裸露的mRNA容易被体内普遍存在的RNase的降解,mRNA需要封装在递送平台中以增强其内体逃逸效率,这在随后的抗原呈递过程中起着至关重要的作用。多功能递送策略赋予mRNA靶向特定器官和细胞的能力,可以有效激活APC,并通过佐剂作用刺激免疫相关信号通路,从而显著提高抗肿瘤功效。一般来说,合适的递送系统有助于克服基于mRNA的癌症免疫治疗的瓶颈,例如靶向递送、提高转染效率和增强免疫反应强度。目前用于mRNA递送的技术平台包括LNP、水凝胶材料、聚合物递送和基于肽的递送方式,如下图所示。
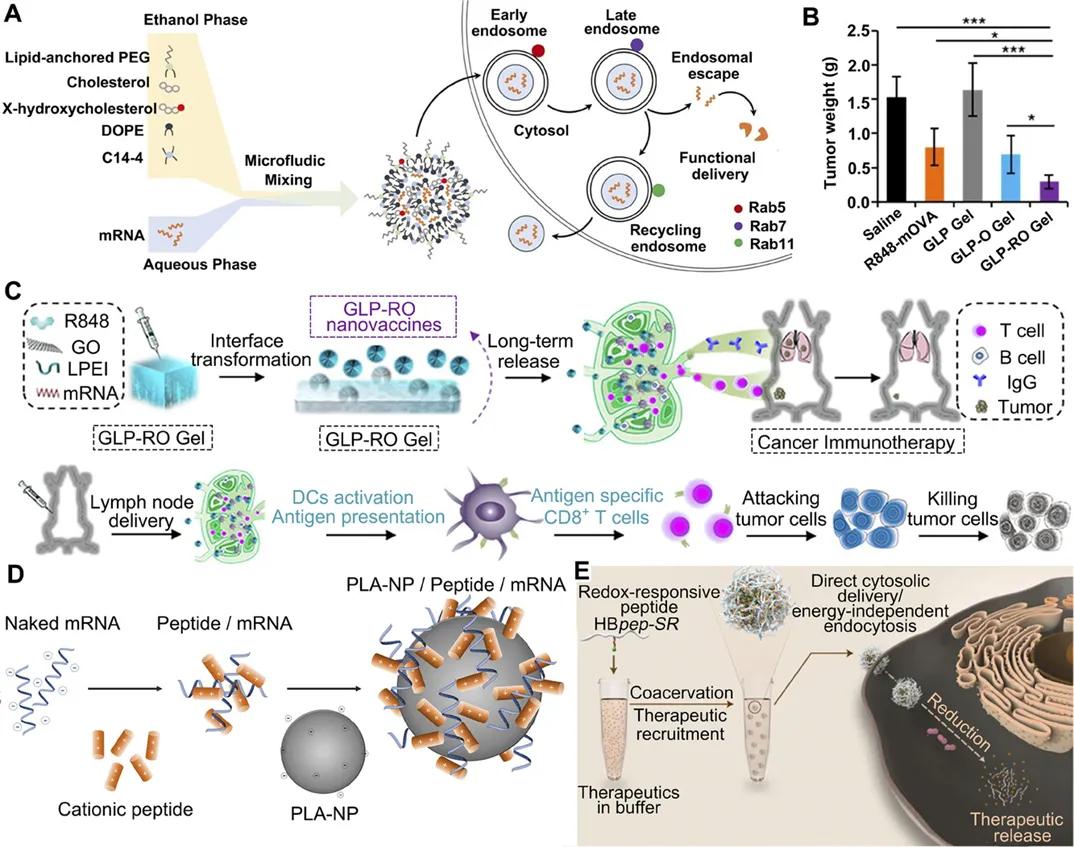
▲图3 用于mRNA递送的 LNP、水凝胶、聚合物和基于肽递送示意图。
A. 具有羟基胆固醇替代的工程LNP,用于将 mRNA 传递至T细胞癌症免疫治疗。B. GLP-RO Gel和其他组处理后肿瘤重量变化图。C. 使用聚乙烯亚胺和GO水凝胶制备GLP-RO凝胶用于持久癌症免疫治疗。D. 用聚乳酸NP和CPP将 mRNA 递送至 DC 中以诱导有效免疫反应。E. 用于 mRNA 胞质递送的相分离肽,具有更高的稳定性和高转染效率。
总之,该综述详细总结了将 mRNA 精确运输到肿瘤细胞、DC、T 细胞、B 细胞和巨噬细胞等特定器官和细胞的研究,提出了基于mRNA 的癌症免疫疗法的临床转化将受益于 mRNA 设计中生物化学的深度整合,同时在靶向 mRNA 递送中采用材料和纳米技术有可能解决当下临床中面临的诸多挑战。由于篇幅有限,这里不再过多介绍,感兴趣的朋友可以详细阅读原文,了解最近mRNA癌症疗法领域的前沿进展和临床应用。
原文链接:
https://onlinelibrary.wiley.com/doi/full/10.1002/EXP.20210146
本公司产品推荐:
1.1184172-53-9 https://www.bicbiotech.com/product_detail.php?id=5520
2.1214323-32-6 https://www.bicbiotech.com/product_detail.php?id=5521
3.876919-08-3 https://www.bicbiotech.com/product_detail.php?id=5522
4.1147014-97-8 https://www.bicbiotech.com/product_detail.php?id=5523
5.1056264-66-4 https://www.bicbiotech.com/product_detail.php?id=5524




