靶向蛋白降解(TPD)是近年来新药研发最具革命性的技术方向之一,以 PROTAC 为代表的降解技术突破了传统小分子抑制剂的局限,实现 “清除致病蛋白” 的治疗目标。但传统 PROTAC 高度依赖 E3 泛素连接酶,存在配体稀缺、适用靶点有限、成药性不佳等瓶颈。
近日,西班牙研究团队在《Nature Communications》发表重磅研究“Expanding the targeted protein degradation approach with small molecule chimeras directed to the 26S proteasome”,成功开发26S靶向泛素非依赖降解剂(26S-UIDs),绕过 E3 连接酶,直接将靶蛋白递送至 26S 蛋白酶体降解,为靶向蛋白降解领域开辟全新赛道。

传统 PROTAC 的核心局限
经典 PROTAC 分子如同 “分子桥梁”,一端结合致病靶蛋白,一端招募 E3 泛素连接酶,通过泛素化标记靶蛋白,最终由26S蛋白酶体识别并降解。尽管PROTAC已在临床展现潜力,但其固有缺陷难以突破:
- E3 配体极度稀缺:可用于构建PROTAC的 E3 泛素连接酶配体数量极少,极大限制分子设计空间。
- 依赖泛素化过程:要求靶蛋白具备可修饰的赖氨酸位点,大量无合适位点的蛋白无法被降解。
- 组织适用性受限:E3 连接酶在不同组织中的表达量与活性差异大,导致部分靶点降解效率低下。
- 成药性挑战:PROTAC 分子量大、溶解度差,口服吸收与体内代谢难以优化。
这些问题促使学界寻找不依赖 E3、不依赖泛素化的新型降解策略。
26S-UIDs:颠覆性的降解新机制
研究团队跳出传统思路,选择26S 蛋白酶体调控蛋白 USP14作为招募靶点,构建全新小分子降解体系 26S-UIDs,核心原理完全区别于 PROTAC:
双端结合:小分子嵌合体一端结合靶蛋白,一端特异性结合 USP14。
直接定位:将靶蛋白精准牵引至 26S 蛋白酶体的 ATP 酶马达附近。
非泛素依赖:无需 E3 连接酶参与,无需泛素化修饰,直接触发蛋白酶体对靶蛋白的解折叠与降解。USP14 是 26S 蛋白酶体调控因子,位于蛋白酶体调节颗粒基部,靠近 ATP 酶通道,是理想的锚定位点。研究团队基于 USP14 小分子配体 IU1 家族优化,筛选出高亲和力、低抑制活性的配体317,大幅提升降解效率。
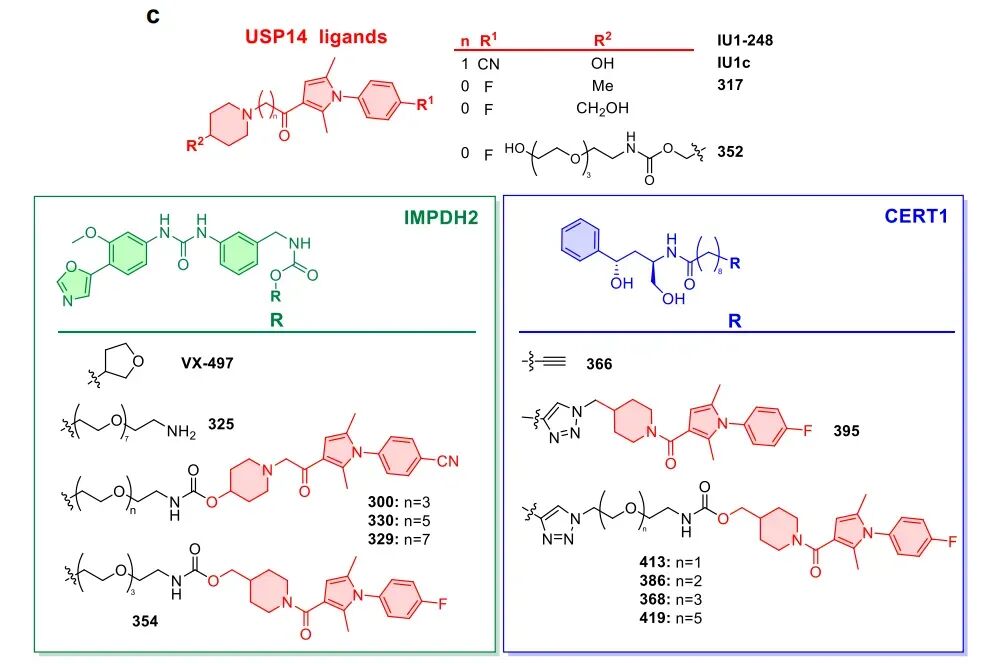
两大抗癌靶点验证:高效、特异、机制确凿
研究选取IMPDH2(白血病、淋巴瘤关键靶点)与CERT1(乳腺癌耐药调控靶点)作为模型,完成系统性功能验证,结果极具说服力。
IMPDH2 是鸟嘌呤核苷酸从头合成的限速酶,在白血病、淋巴瘤及多种实体瘤中高表达,与肿瘤进展、化疗耐药密切相关,目前仅有极少数降解剂报道。研究人员以 IMPDH2 抑制剂 VX-497 为靶头,以 USP14 配体 IU1-248 及其衍生物为招募端,通过不同长度的 PEG 连接子构建了一系列嵌合体。细胞实验显示,优化后的分子354在500–1000 nM浓度下即可实现 IMPDH2 的完全清除,降解效果显著优于早期分子。机制研究证实:IMPDH2 的降解可被蛋白酶体抑制剂逆转,但不受泛素激活酶抑制剂 MLN7243 影响;在 USP14 敲除细胞中,降解作用完全消失。上述结果直接证明,26S-UIDs 以USP14 依赖、泛素非依赖、蛋白酶体依赖的方式实现靶蛋白清除。
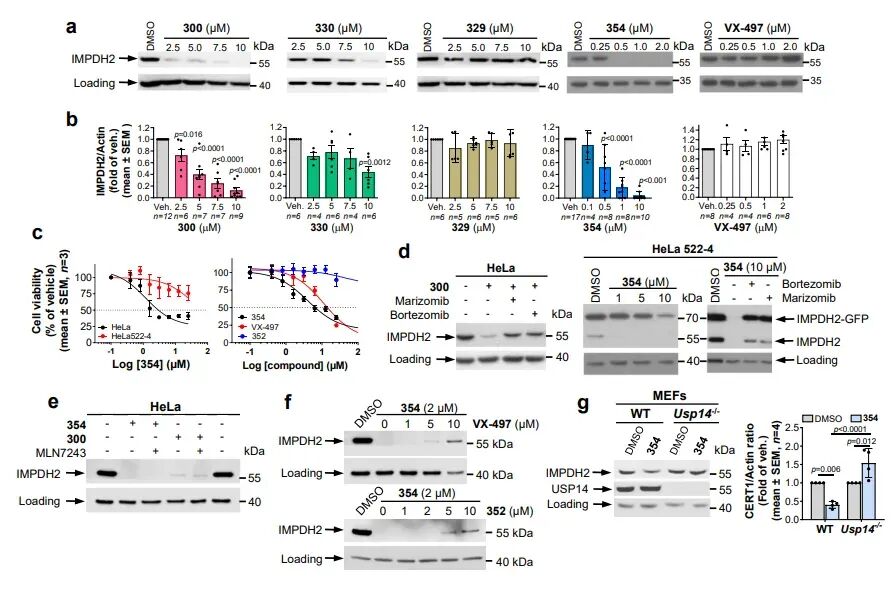
CERT1 是神经酰胺转运蛋白,负责将神经酰胺从内质网转运至高尔基体合成鞘磷脂,其高表达会降低细胞内促凋亡神经酰胺水平,介导乳腺癌等肿瘤的化疗耐药,此前尚无针对 CERT1 的降解剂报道。本研究以 CERT1 的 HPA 家族拮抗剂为靶头,同样采用 USP14 配体 317 构建了 5 种 26S-UIDs。实验结果显示,最优分子368在16–24 小时内即可显著降解 CERT1,且降解机制与 IMPDH2 完全一致:依赖 26S 蛋白酶体、依赖 USP14、不依赖泛素化。脂质组学分析证实,CERT1 降解会导致细胞内C14–C20 链长的促凋亡神经酰胺显著累积,并可增敏 HER2 阳性乳腺癌细胞对拉帕替尼的敏感性,提示该策略在克服肿瘤耐药方面具有重要应用价值。
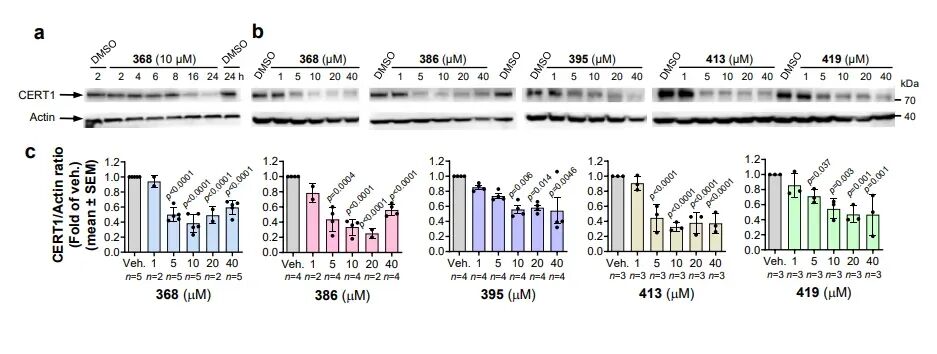
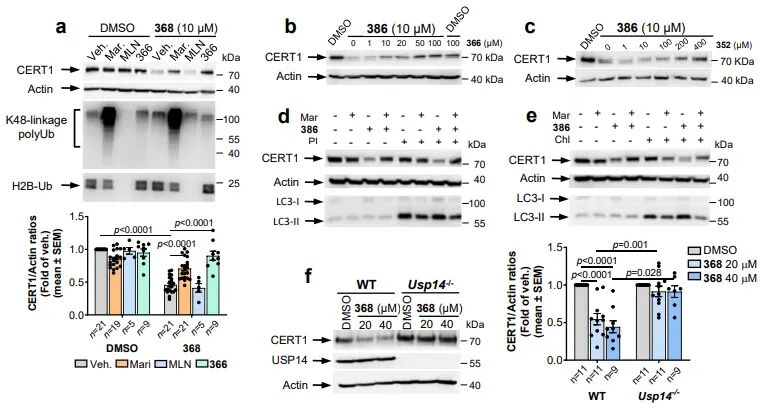
三元复合物验证
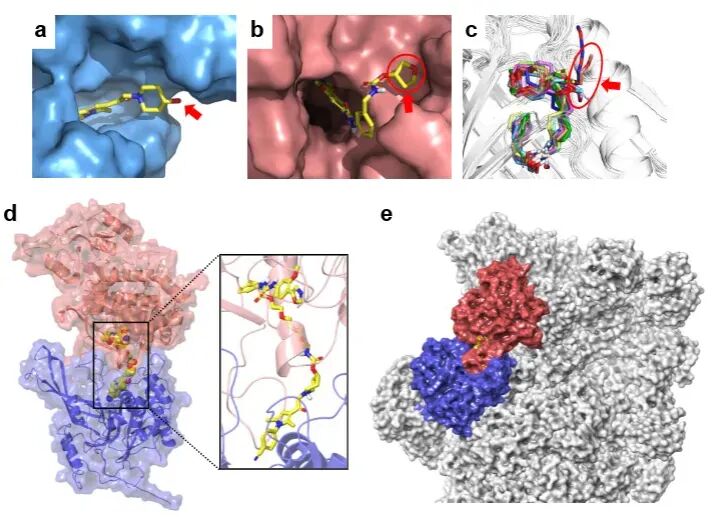
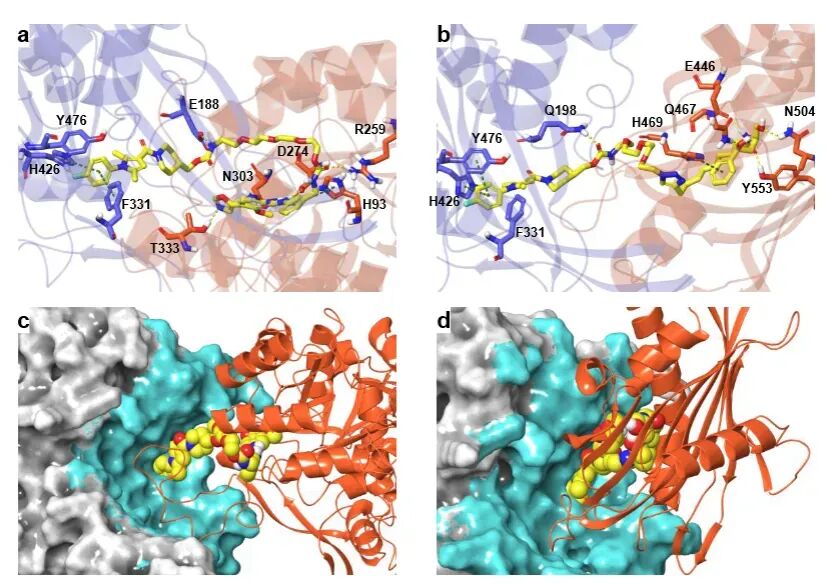
为进一步解析分子机制,研究团队通过表面等离子共振(SPR)、Pull-down 实验与计算机模拟,证实 26S-UIDs 可介导USP14–嵌合体–靶蛋白三元复合物的形成,且该复合物的空间构象与 26S 蛋白酶体的结构完全兼容,不会产生空间位阻。
与传统 PROTACs 不同,26S-UIDs 的降解效率不完全依赖连接子长度与界面能量,展现出更宽松的分子设计空间。
26S-UIDs 技术的核心优势
总体而言,本研究成功建立了一套不依赖 E3 泛素连接酶、不依赖底物泛素化的全新靶向蛋白降解平台。26S-UIDs 以小分子形式直接招募 26S 蛋白酶体,突破了传统 PROTACs 的核心限制,具备成药性更优、适用靶点更广、作用机制新颖等优势。对 IMPDH2 与 CERT1 的成功验证,不仅为肿瘤治疗提供了全新候选分子,更证明该策略具备高度普适性,未来可拓展至更多致病蛋白的降解。
免责声明:本文仅作知识交流与分享及科普目的,不涉及商业宣传,不作为相关医疗指导或用药建议。文章如有侵权请联系删除。
本公司产品推荐:
1.389628-28-8 https://www.bicbiotech.com/product_detail.php?id=6527
2.1071608-51-9 https://www.bicbiotech.com/product_detail.php?id=6528
3.193354-13-1 https://www.bicbiotech.com/product_detail.php?id=6529
4.102331-54-4 https://www.bicbiotech.com/product_detail.php?id=6530
5.175281-76-2 https://www.bicbiotech.com/product_detail.php?id=6531




