2024年4月26日,美国食品药品监督管理局(FDA)宣布批准X4 Pharmaceuticals公司研发的新分子实体药物Xolremdi(有效成分:Mavorixafor)上市,Xolremdi是一种选择性CXC趋化因子受体4(CXCR4)拮抗剂,适用于 12岁及以上的WHIM综合征(疣、低丙种球蛋白血症、感染和骨髓粒细胞缺乏症)患者,以增加循环中的成熟中性粒细胞和淋巴细胞的数量。Xolremdi是第一种专门用于WHIM综合征患者的疗法。

图1:FDA已批准Xolremdi上市
WHIM综合征是一种罕见的先天免疫缺陷性疾病,表现为人乳头瘤病毒(HPV)所导致的疣、低丙种球蛋白血症、细菌感染以及无效生成性慢性粒细胞缺乏的四联症。WHIM综合征患者的特征性是血液中中性粒细胞和淋巴细胞减少,并经历严重和/或频繁的感染,是一种常染色体显性遗传病。据估计,大约每 500万活产婴儿中就有1例,医学文献中已报道了约60个病例。美国目前至少有1,000人被诊断出患有WHIM综合征,此外,欧洲、日本及我国都有WHIM综合征的病例报道,男女均可累及。
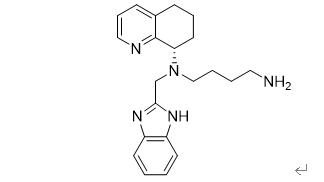
图2: Xolremdi结构
现阶段研究已证实WHIM综合征是由CXCR4基因的杂合突变所引起,导致白细胞从骨髓进入外周循环的动员受损。CXCR4表达于大部分成熟白细胞亚型以及造血祖细胞上,具有淋巴细胞趋化特性。CXCR4的配体,骨髓基质细胞衍生因子(SDF-1,亦称CXCL12)在造血干细胞归巢及休眠方面起重要作用。
当CXCL12与CXCR4结合,信号转导激活下游效应器,如AKT及细胞外信号调节激酶(Erk),通过钙离子流动触发细胞滞留。WHIM患者中CXCR4突变使其活性增强,致使成熟中性粒细胞从骨髓释放延迟,外周血白细胞减少,而存留在骨髓的成熟白细胞则会进一步凋亡,故而患者血液中中性粒细胞和淋巴细胞减少。
因此Xolremdi是一种口服生物活性CXCR4拮抗剂,可以阻断抑制配体CXCL12与其受体CXCR4的结合,提高循环中的成熟中性粒细胞和淋巴细胞的数量,改善WHIM患者症状。
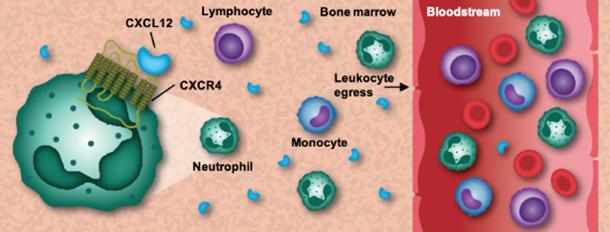
图3:CXCR4 通路调节白细胞从骨髓到外周血的动员
FDA批准Xolremdi的依据是关键的4WHIM 3期临床试验结果,该试验于2019年10月24日开始实施,是一项全球性、随机、双盲、安慰剂对照、为期52周的多中心研究,评估了Xolremdi在31名12岁及以上确诊为WHIM综合征患者中的疗效和安全性。
31名患者按1:1比例随机接受安慰剂(17人)或Xolremdi(14人)治疗,每天一次,疗程52周。Xolremdi治疗WHIM综合征患者的疗效基于中性粒细胞绝对计数(ANC)的改善、淋巴细胞绝对计数(ALC)的改善以及感染的减少来确定。在4WHIM试验中,Xolremdi治疗显示中性粒细胞绝对计数(TAT-ANC)超过阈值(≥500个细胞/微升)的时间比安慰剂延长,淋巴细胞绝对计数(TAT-ALC)超过阈值(≥1000个细胞/微升)的时间比安慰剂延长。在安全性方面,与接受安慰剂治疗的患者相比,接受Xolremdi治疗的患者的年感染率降低了60%。4WHIM试验达到了其主要终点和关键次要终点,并且在试验中总体耐受性良好,没有报告与治疗相关的严重不良事件,也没有因安全事件而停药。
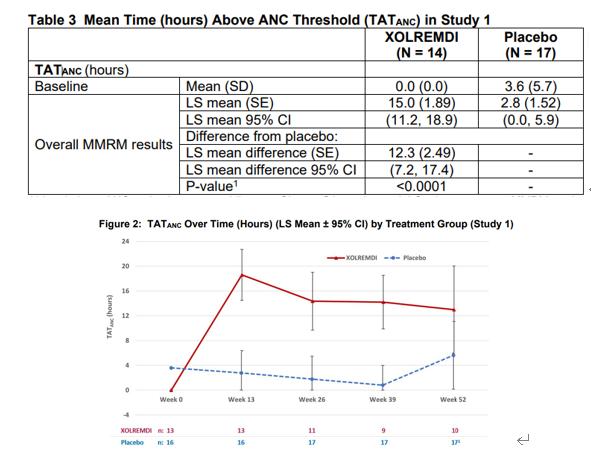
图4: Xolremdi临床试验结果
X4 Pharmaceuticals公司在得到了全球关键性4WHIM 3期临床试验结果的支持后,于2023年9月5日向FDA递交了Mavorixafor治疗WHIM综合征的新药上市申请(NDA),并于2023年10月31日宣布,FDA接受Mavorixafor治疗WHIM综合征的美国新药上市申请的优先审评。下图总结了Mavorixafor从研发到上市过程中所经历的临床研究。
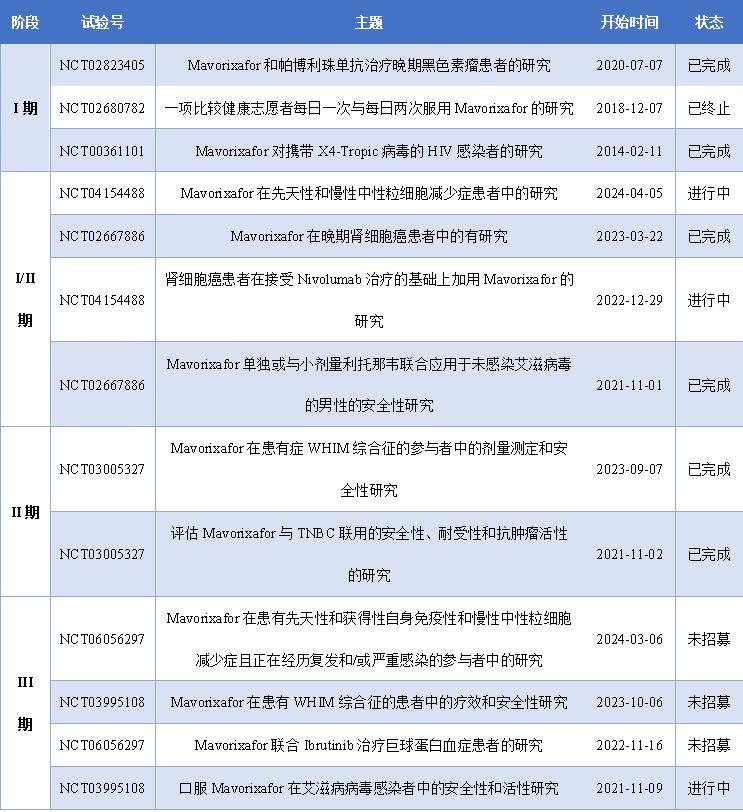
在此之前,针对WHIM综合征患者的治疗主要集中在症状控制上,而不是疾病的根本原因--CXCR4通路的功能障碍。Xolremdi是一种旨在解决CXCR4通路信号传导失调问题的疗法,这种靶向治疗方法的获批,已证明能够提高中性粒细胞和淋巴细胞的绝对数量,增强WHIM患者的抗感染能力。
参考资料:
[1]FDA官网:https://www.fda.gov/
[2]X4 Pharmaceuticals官网:https://www.x4pharma.com/
[3]宋泽亮,师晓东.WHIM综合征的研究进展[J].中国医刊,2016,51(04):28-30.
[4]Drug Bank官网:https://go.drugbank.com/




