5月15日,百时美施贵宝公司(BMS)宣布,美国食品药品管理局(FDA)已加速批准靶向CD19抗原的自体CAR-T细胞疗法Breyanzi ® (lisocabtagene maraleucel; liso-cel)扩大适应症,用于治疗既往接受过两种或两种以上系统疗法的复发性或难治性滤泡性淋巴瘤(FL)成年患者。该适应症是根据应答率和应答持续时间加速批准的,该适应症的继续批准可能取决于确证试验对临床疗效的验证和描述。

这是Breyanzi第四次获FDA批准新适应症。
- 2021年2月,Breyanzi首次在美国获批上市,用于治疗接受过两种或多种系统治疗的复发或难治性大B细胞淋巴瘤(LBCL)成人患者,包括未另有说明的弥漫性大B细胞淋巴瘤(DLBCL)、高级别B细胞淋巴瘤、原发性纵隔大B细胞淋巴瘤和3B级FL。
- 2022年6月24日,Breyanzi 获FDA批准用于二线治疗成人大B细胞淋巴瘤(LBCL),包括弥漫性大B细胞淋巴瘤(DLBCL)、高级别B细胞淋巴瘤、原发性纵隔大B细胞淋巴瘤、3B级FL。
- 2024年3月15日,Breyanzi获FDA加速批准用于治疗复发/难治性慢性淋巴细胞白血病(R/R CLL)或小淋巴细胞淋巴瘤(SLL)成人患者,这些患者之前至少接受过两线治疗,其中包括BTK抑制剂和BCL-2抑制剂。
- 本月末,Breyanzi用于治疗套细胞淋巴瘤(MCL)成年患者的补充生物制品许可申请也将迎来FDA的监管决定。
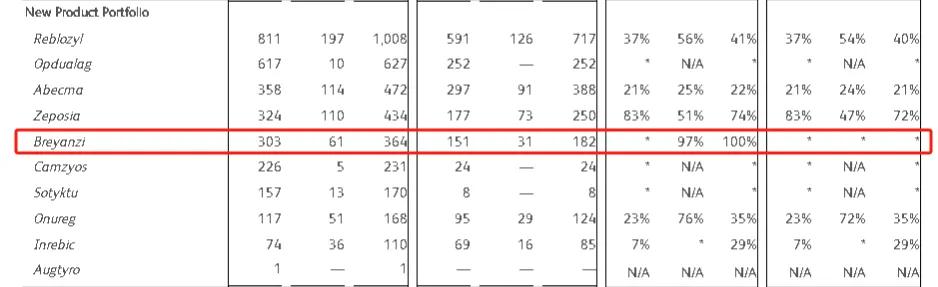
自上市以来,2024Q1Breyanzi销售额1.07亿美元,同比增长51%;2023年Breyanzi销售额3.64亿美元,同比大涨100%;2022年Breyanzi销售额1.82亿美元,2021年为0.87亿美元。上市三年来,已经卖了7.4亿美元(约53.47亿元)。
FL一直被认为是一种不治之症,患者在接受一线治疗后经常复发,而且每次复发后预后都会恶化。尽管在治疗方面取得了进展,但人们仍然需要更多的选择,以提供无治疗间隔期和持久、完全的反应。
这一加速批准是基于2期临床试验TRANSCEND FL的积极结果。TRANSCEND FL (NCT04245839)旨在确定Breyanzi对于复发或难治性非霍奇金B细胞淋巴瘤(包括滤泡性淋巴瘤)患者的疗效和安全性。主要结果指标是总体缓解率,次要结果指标包括完全缓解率、缓解持续时间、无进展生存期和安全性。
结果显示在三线加用Breyanzi治疗并纳入主要疗效分析组 (n=94) 的患者中,总体缓解率(ORR)为95.7%(95% CI:89.5-98.8)。完全缓解率(CR)为73.4%(95% CI:63.3-82.0)。中位缓解持续时间(DOR)未达到(95% CI:18.04-NR),80.9%的反应者在12个月时仍有反应,77.1%的反应者在18个月时仍有反应。
在2023年国际恶性淋巴瘤大会上公布的TRANSCEND FL主要分析结果显示,疗效可评估患者(n=101)的ORR为97%(95% CI:91.6-99.4;单侧p<0.0001),94%的患者达到CR(95% CI:87.5-97.8;单侧p<0.0001)。

Breyanzi具有稳定的安全性,在各项临床试验中,53%的患者出现了任何等级的细胞因子释放综合征(CRS),其中4%的患者出现了大于3级的CRS。中位发病时间为 5天(范围:1-63天)。31%的患者发生了任何级别的神经系统事件(NEs),其中10%的患者发生了级别>3的NEs。NEs发生的中位时间为8天(范围:1-63天)。
百时美施贵宝公司高级副总裁、细胞疗法商务负责人Bryan Campbell说:“Breyanzi是我们细胞疗法产品组合的基石,可为多种B细胞恶性肿瘤提供差异化的治疗方案。今天,Breyanzi获批用于复发或难治性FL的治疗,提供了一种一次性输注即可获得持久缓解的选择,其安全性使其可以在美国越来越多的认证治疗中心的住院和门诊环境中进行给药和监测。”




