近几年围绕“3D细胞培养”公开发表的文章或评论数量上升迅猛,3D细胞培养衍生的类器官技术同样成为研究学者的利器。
3D细胞培养,又称三维细胞培养,是指将动物细胞与具有三维结构的支架材料共同培养,使细胞能够在三维立体的空间生长、增殖和迁移,构成三维的细胞-细胞或细胞-载体复合物,从而更好地模拟细胞在体内的生长环境。
适用于:分子和细胞生物学分析,在动物和细胞水平之间,广泛应用于功能组织诱导、疾病模型建立、药物筛选、抗炎试验、临床端研究等多个方面的研究。
类器官(Organoids)是一种在体外环境下培养而成的具备三维结构的微器官,具有类似于真实器官的复杂结构,并可以部分模拟来源(干细胞、肿瘤组织、病人来源等)组织或器官的生理功能。截至目前已有10多种不同组织、疾病模型及模拟发育的类器官问世。类器官作为一项重大的技术突破,已被公认为生物科学领域研究的重要工具,并具有重要的临床应用价值。
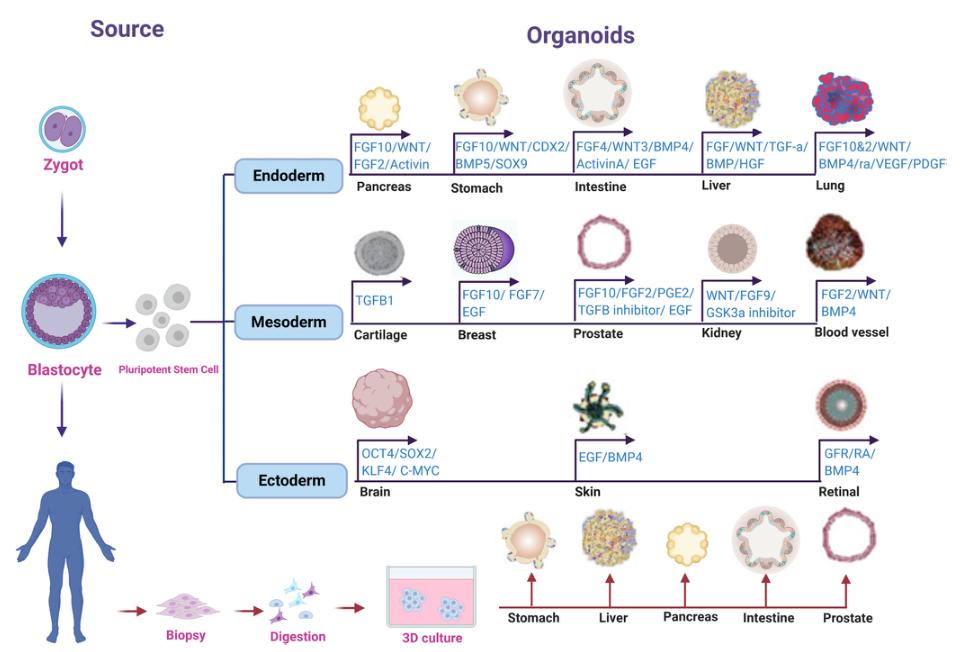
参考文献:Organoid technology Current standing and future perspectives
从类器官的定义和来源来看,是将多能干细胞或患者来源的肿瘤组织等进行3D细胞培养,从而形成相应器官的自组织,并具有自我更新和自我组织的能力,故又称“平皿里的器官”。类器官属于3D细胞培养物,包含器官特异性细胞类型,可以表现出器官的空间组织和复制器官的某些功能。类器官重现了一个生理上高度相关的系统,在三维体系下可以研究复杂的问题。例如,疾病发作、组织再生和器官之间的相互作用。
这些由大量细胞簇聚而成的类器官,虽然在很多方面能模拟真实器官内部结构,但某些与真实器官功能和发育紧密相关的结构特性至今还无法拥有,如缺乏血管系统,这是人体器官生长发育中获取能量的重要结构。因此,目前为止,类器官还不能称为真实器官的“缩小版”,仍然是微型和简单的器官模型。
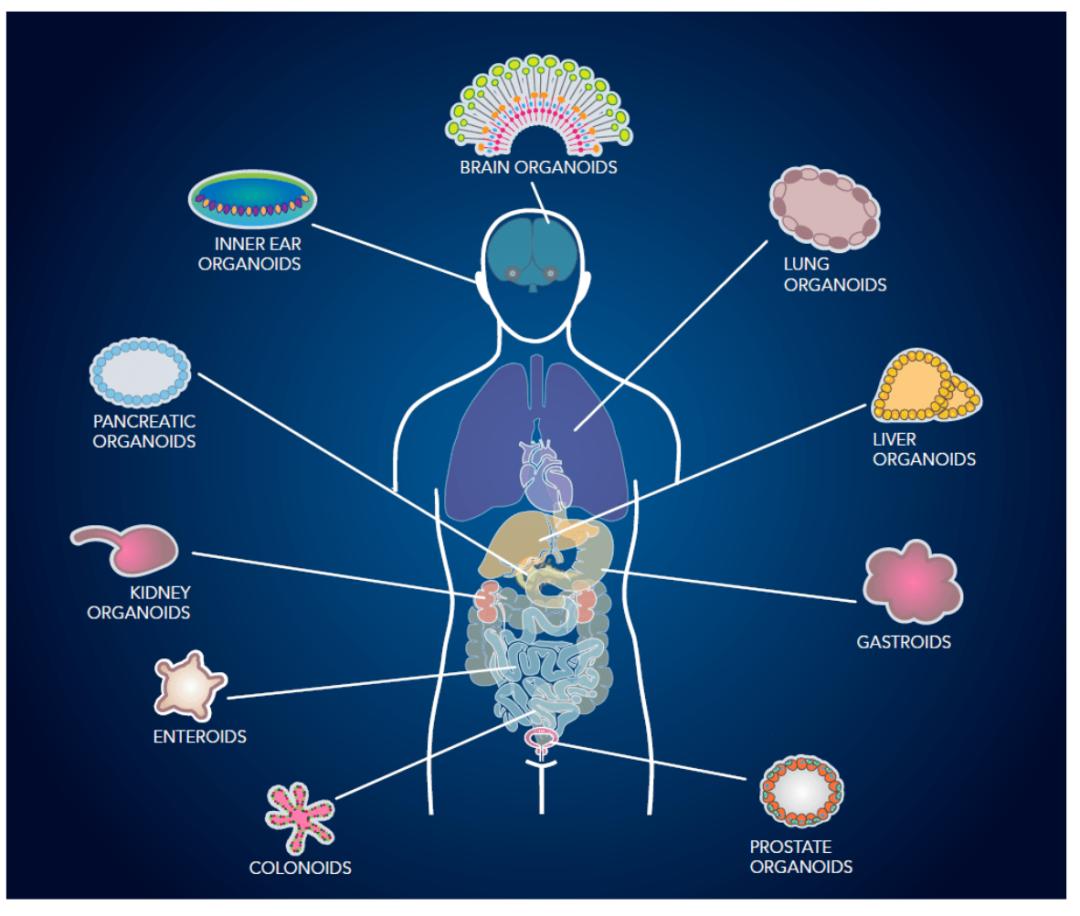
目前类器官的培养主要是指上皮细胞类器官, 如消化道上皮细胞、乳腺上皮细胞、皮肤上皮细胞、肺泡上皮细胞等, 大部分的类器官中只有上皮细胞, 不含有成纤维细胞、免疫细胞、血管细胞等周围基质细胞。
类器官培养如何进行
如常规的细胞培养有什么不同?
如何实现三维细胞培养:
固体支架三维培养:组织工程支架作为组织工程的平台,不仅提供了细胞生长的框架,使之形成特定的组织或器官形状;而且作为细胞外基质成分之一,是细胞间信号传导和相互作用的媒介,同时也是细胞生长所必需的生物活性剂。
磁力悬浮三维培养:美国莱斯大学和德克萨斯大学M.D. Anderson癌症中心的研究人员开发出一种生物装配器(bioassembler)。这个系统使用磁力让细胞悬浮,并促使细胞生长成三维的形状。尤其适于培养肝脏和心脏这种细胞密度比较大的实体器官。
水凝胶三维培养:将细胞培植在一定的细胞外基质中 , 细胞外基质(extracellularmatrix, ECM)蛋白充当生长支架。美国布朗大学的生物工程师 Jeffrey Morgan 利用琼脂糖开发出一种细胞三维培养皿。将融化的琼脂糖制成微型培养板(micro-moulds),等琼脂糖凝固之后,再将这种琼脂糖材料放置到普通的培养板里。再在培养板里加入细胞和培养基,由于重力的作用,细胞会沉积到琼脂糖培养板里,彼此聚集在一起,形成球形的多细胞团块。
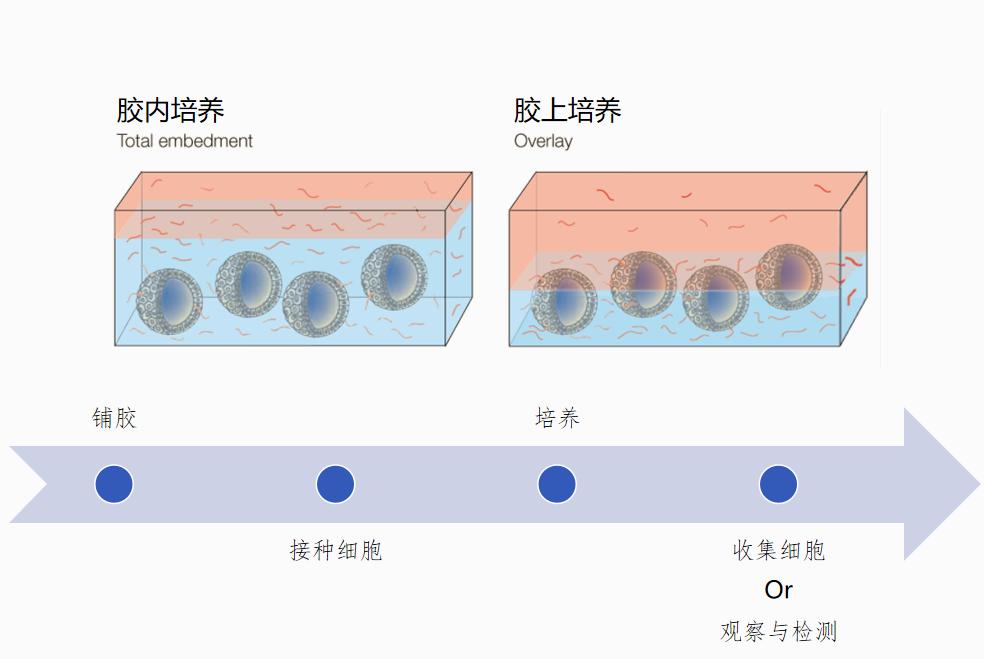
1)三维结构:类器官培养在3D结构中进行,更好地模拟细胞在体内的空间排列和相互作用,而常规细胞培养通常是在平面的2D环境中。
2)细胞类型多样性:类器官可以包含多种类型的细胞,更好地重现器官的复杂性,而传统的细胞培养通常涉及单一细胞类型。
3)微环境模拟:类器官培养更强调在体微环境的模拟,包括细胞间相互作用和基质组成,而2D培养则较少考虑这些因素。
4)用途与应用:类器官培养适用于研究复杂的细胞相互作用、疾病模型、药物筛选等,而常规的2D细胞培养更多用于基础的细胞生物学研究。
5)技术复杂度和成本:类器官培养技术通常更复杂、成本更高,需要专业的技术和材料。
在3D细胞培养中,有许多不同的方案和方法可供选择。以下是一些常见的3D细胞培养方案或方法:
多孔支架法:使用多孔结构的材料(如海绵、凝胶或聚合物支架)来提供细胞生长的三维支撑结构。这种方法可以通过调节支架的孔隙度和形状来控制细胞的分布和生长。
多孔支架法是一种常用的制备3D细胞培养基质的方法。该方法在一块支架上构建具有细小孔隙结构的三维基质,在这些孔隙内细胞可以定植和生长。多孔支架可以通过生物降解或非生物降解材料制备,具有良好的生物相容性和组织相似性,能够提供细胞生长所需的支持和适宜的微环境。
自组装法:利用细胞自身的黏附力和相互作用力,在无需外部支持的情况下形成三维结构。这可以通过调整细胞密度、细胞类型和培养条件来实现。
自组装法是一种利用多种细胞自发性组装形成组织结构的技术。在这种方法中,细胞通过粘附分子或特定的细胞-细胞相互作用自行组装成具有特定结构和功能的组织。这种方法可以制备复杂的多细胞体系,并在体外重建组织结构和生理功能。
3D打印法:使用3D打印技术将细胞和支架材料按照设计的结构和形状进行打印组装。这种方法可以制造出复杂和定制化的3D细胞构造。
3D打印法是一种将细胞和生物材料以逐层方式打印形成3D结构的技术。通过使用3D打印机,可以按照预设的设计和模型,将生物材料和细胞逐层叠加打印,最终形成具有复杂结构的组织或器官模型。这种方法可以精确控制细胞分布和支架的形状,实现定制化的3D细胞培养。
悬浮培养法:将细胞以悬浮状态培养在无支撑物的培养基中。这种方法可以使细胞自由地形成三维聚集体,如球体或团块。
悬浮培养法是一种将细胞悬浮在培养基中进行三维培养的方法。在这种方法中,细胞可以在液体环境中自由悬浮,通过细胞自主的自组装或微环境调控形成3D结构。悬浮培养法常用于培养复杂的多细胞体系,如肿瘤球体等。
微流控技术:利用微流体设备和微流控芯片的特殊纹理和结构,控制细胞在三维空间中的位置和生长。这种方法可以模拟体内的微环境,实现更精确和可控的细胞培养。
微流控技术是一种利用微流道和微阀门等微加工技术来精确控制细胞和流体的方法。通过微流控技术可以实现对细胞和培养环境的精确控制和调整,模拟复杂的生物体内环境。这种方法常用于研究细胞间相互作用、细胞迁移和组织重塑等。
剥蚀法:将细胞培养在具有特殊性质的材料或衬底上,然后使用特定的剥离技术将细胞构造剥离下来。这种方法可以制备出较薄的3D细胞结构。
剥蚀法是一种将组织或器官外层的细胞剥离或去除,然后将剥离的细胞重新组装成3D结构的方法。通过剥蚀法可以重塑组织的形态和结构,并研究细胞的再分化和自组装能力。
组织工程法:利用组织工程学原理和技术,将细胞和生物材料结合起来,形成具有组织类似结构和功能的3D构造。这种方法可以通过多种组织的联合培养来模拟和重建复杂的组织和器官。
组织工程法是将生物材料与细胞结合,以构建具有生物学功能的组织结构。通常,组织工程法将生物材料作为支架或载体,用于促进细胞的附着、增殖和分化。通过合理地选择和设计生物材料,可以改善细胞培养的环境和刺激效应,促进组织的再生和修复。




